
Питер Дашак из EcoHealth, Ральф С. Барик и Ши Чжэнли-Ли
Когда ученые-исследователи получают гранты, в частности от федерального правительства, они должны продемонстрировать, что деньги были использованы именно в тех целях, на которые они были выделены. В результате ожидается, что ученые и врачи опубликуют результаты этого исследования. Эти публикации оставляют неуничтожимый след в истории.
Исследовательская карьера строится на доказательстве того, что работа, выполненная ученым, продвинула поиски знаний, и ученые делятся этой информацией с коллегами ― и все это для развития науки.
Отцы-основатели признали важность такой работы и предоставили защищенное конституцией США право людям, которые продвинули науку в достаточной степени, чтобы сделать изобретение, которое будет признано полезным для человечества. Право выдавать патенты изобретателям находится в ведении законодательной ветви власти федерального правительства, также известного как Конгресс. Таким образом, эти патенты обеспечивают неуничтожимый отчет о том, что именно было обнаружено, и кем.
По этим причинам мы теперь рассмотрим лишь некоторые из публикаций и патентных свидетельств того, что SARS-CoV-2, также как и другие вирусы, является результатом исследования усиления функциональности, что записано в опубликованных исследованиях, патентах, и, как мы увидим в этой и следующей главах, в финансировании.
Содействовать прогрессу науки и полезных искусств, обеспечивая на ограниченное время авторам и изобретателям исключительное право на их соответствующие сочинения и открытия.
- Конституция США, статья I, раздел 8, § 8.
1974: Первый известный искусственно измененный вирус
Насколько мне известно, первым [1] генетически измененным (при помощи усиления функциональности) вирусом стал Qß-фаг в 1974 году [2]. Это исследование усиления функциональности, как и многие другие проекты, последовавшие за этими исследователями, было оплачено грантами Федерального исследовательского проекта NIH (ROI).
1985: Ранние работы Барика с рекомбинацией коронавирусов
Насколько мне известно, Ральф Барик начал работать с коронавирусами, обнаруженными у мышей, еще в середине 1980-х годов. В 1985 году, когда он работал в Калифорнийском университете в Лос-Анджелесе (UCLA), он и его коллеги из Центра медицинских наук Техасского университета в Хьюстоне (UTHSCH) провели исследование рекомбинантных вирусов, включая коронавирусы [3]. Это исследование было оплачено несколькими грантами, включая грант Национального научного фонда (PCM-4507) и грант на исследования Службы общественного здравоохранения США (AI 19244). Служба общественного здравоохранения США является подразделением Министерства здравоохранения и социальных служб США (HHS).
1987: Патент предоставлен доктору Кэри Б. Маллису на полимеразную цепную реакцию (ПЦР).
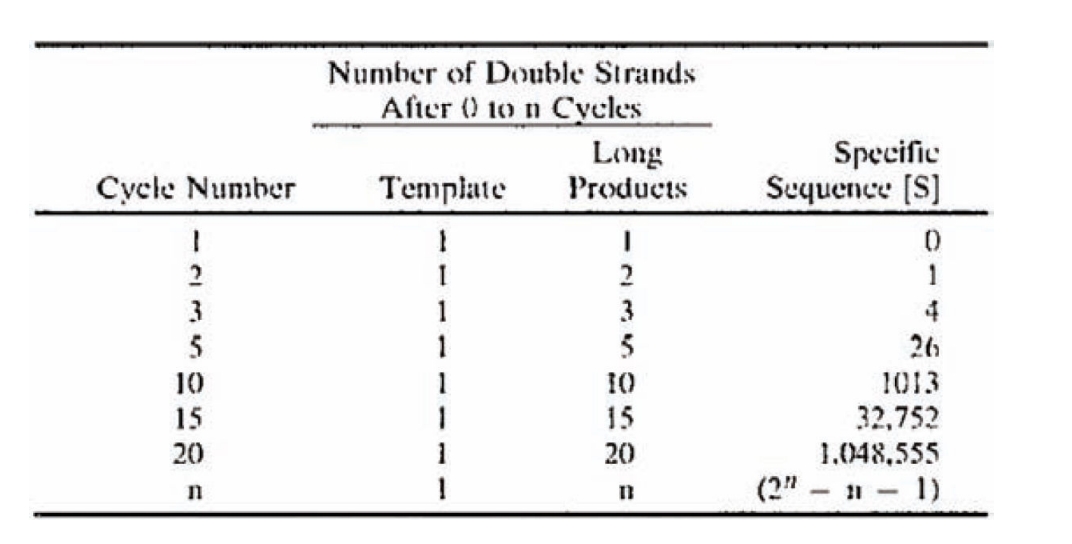
Патент № 4683195 был выдан Маллису и другим на «процесс обнаружения присутствия или отсутствия по крайней мере одной конкретной последовательности нуклеиновых кислот в образце, содержащем нуклеиновую кислоту или смесь нуклеиновых кислот».
Четкий обзор этого патента показывает, что Маллис не превышал пятнадцати-двадцати циклов ПЦР [4] для идентификации генетического материала.
1994: Флеминг представляет теорию воспаления и заболеваний сердца
В 1994 году на собраниях Американской кардиологической ассоциации я впервые представил свою теорию воспаления и заболеваний сердца. Я повторял свое выступление в 1995 году, и к 1999 году моя теория стала частью учебника кардиологии [5]. Схема этой теории показана в приложении. Теория, объясняющая воспаление и тромботические хронические заболевания [6], позже была обсуждена в 20/20 [7] и других программах. Я опубликовал информацию о роли многих факторов, в том числе бактерий и вирусов, участвующих как в воспалении, так и в образовании тромбов ― о процессе, который с тех пор я называю воспалительно-тромбозной реакцией (ITR). Именно эта ITR несет ответственность за COVID-19 и смертельные случаи среди людей, которых не лечат от ITR [8].
2000: Создание ДНК из РНК ― обратная транскрипция: уроки, извлеченные из ВИЧ
В начале 2000 года мы узнали, что исследователи из Испании, о работе которых сообщил Пол Алквист из Университета Висконсина, показали, как сочетание комплементарной кодирующей цепи ДНК (кДНК) с экспрессией РНК в ядре позволило исследователям разработать синтетический вирус [9]. Комплементарная ДНК ― это одноцепочечная молекула ДНК, которая химически состоит из одноцепочечной РНК.
Для этого требуется фермент, называемый обратной транскриптазой (ОТ). ОТ делает возможным создание кДНК из РНК. Во время конструирования этого инфекционного кДНК вируса белок-шип вируса был заменен генами белка-шипа другого вируса. В результате был получен химерный вирус (усиление функциональности), инфицировавший желудочно-кишечный тракт свиней. Исследователи пришли к выводу, что теперь это можно использовать для собак, кошек и людей:
Эта кДНК также может быть основой тканеспецифической системы экспрессии, которая может использоваться у четырех видов ― человека, свиней, собак и кошек ― путем замены гена S, включенного в кДНК, геномом коронавируса, инфицирующего целевые виды. Ожидается, что с помощью этой процедуры будут созданы либо полностью инфекционные вирусы, либо, по крайней мере, частично компетентные изоляты, способные экспрессировать чужеродные гены, ― и те, и другие представляют практический интерес [10].
2000: Создание инфекционного передаваемого вируса
После получения финансирования от NIH (грант AI 239476), Барик и другие «улучшили» вирус трансмиссивного гастроэнтерита (TGEV):
Доступность инфекционных структур TGEV, очевидно, принесет пользу исследованиям всех аспектов биологии и патогенеза TGEV, включая анализ репликазы коронавируса и несколько спорных процессов транскрипции, которые управляют экспрессией мРНК субгеномной длины (17, 40, 42, 43) [11].
Барик отметил, что инфекция, вызванная синтетической (произведенной человеком) кДНК, была неотличима от вызванной природным вирусом:
Эти данные показывают, что вирусы, полученные из инфекционных структур кДНК, имели фенотипы, неотличимые от фенотипов TGEV дикого типа в клетках свиней [выделение добавлено] [12].
Из этого исследования ясно, что Барик и другие предвидели возможность дальнейшего манипулирования / создания ДНК:
Наш подход, однако, может предоставить средства для обращения к функции больших блоков ДНК, таких как островки патогенеза, или для непосредственного конструирования хромосом, которые содержат большие интересующие нас кассеты генов (12).
2001: Другие демонстрируют способность генерировать коронавирусы с помощью рекомбинантной (генетической) инженерии
В 2001 году группа немецких исследователей показала, что они тоже могут продуцировать инфекционный коронавирус, используя вирус коровьей оспы [13]. (Вирус коровьей оспы ― это линейный двухцепочечный ДНК-вирус. Он является источником современной противооспенной вакцины). Эти исследователи не только показали, что они могут создать инфекционный коронавирус, но также что они могут выделять его в клетках MRC-5 [14].
Чтобы создать рекомбинантный организм, интересующий ген необходимо сначала выделить и удалить с помощью рестрикционных ферментов [15]. Эти ферменты работают как «молекулярные ножницы», разрезая ДНК с обеих сторон интересующего нас гена. Затем фрагмент ДНК лигируют (присоединяют) к ДНК вектора.
Исследователи отметили преимущество этого подхода обратной генетики:
Классический подход теперь можно дополнить обратным генетическим подходом. Более того, описываемая нами система в принципе также облегчает анализ репликации коронавируса, независимо от жизненного цикла вируса и без необходимости инфицирования через рецепторы. Таким образом, он может быть очень полезным при анализе взаимодействия вируса с клеткой-хозяином в контексте репликации, транскрипции, сборки и высвобождения вируса.
Во-вторых, описываемая нами система дополнит существующие методы получения рекомбинантных коронавирусов (Masters, 1999; Almazán et al., 2000; Yount et al., 2000) и значительно продвинет анализ патогенеза коронавируса. С доступными в настоящее время системами должно быть возможно быстрое создание большой коллекции генетически модифицированных коронавирусов; например, внутри- и межвидовые химерные вирусы, вирусы с инактивацией или удалением генов и вирусы с ослабляющими модификациями или дополнительными функциями. Фенотипы, связанные с этими модификациями, по крайней мере те, которые не являются летальными, затем могут быть протестированы на животных моделях инфекции. В частности, это должно дать важную информацию о взаимосвязи между коронавирусной инфекцией и иммунным ответом.
Наконец, представленные нами результаты также должны способствовать разработке коронавирусных векторов для экспрессии чужеродных белков. В долгосрочной перспективе мы полагаем, что экспрессия нескольких субгеномных мРНК в инфицированных коронавирусом клетках может сформировать основу векторной системы, которая позволяет экспрессировать несколько единиц транскрипции, каждая из которых кодирует чужеродный белок. Эти особенности и автономность репликации РНК коронавируса затем могут быть использованы при разработке нового класса векторов РНК-вакцин. (Bredenbeek & Rice, 1992; Mandl et al., 1998) [16]. [выделение добавлено.]
2001: Барик и его коллеги подали заявку на патент на манипулирование генами
К маю 2001 года Барик и Йонт (Yount) подали заявку на патент, позволяющий им контролировать и получать прибыль от генетических манипуляций с растениями, животными, бактериями и вирусами, включая коронавирусы. Патент был выдан 15 июля 2003 г. Этот патент включал исследования, проведенные при финансовой поддержке налогоплательщиков США [17].

2003: Создание коронавируса
В 2003 году Барик и другие опубликовали исследование [18], финансируемое грантами NIH AI23946, GM63228 и AI26603, показав, что они могут «спасти» вирусы SARSCoV Urbani с помощью обратной генетики [19]. Взяв сегменты кДНК и перекрыв их, они смогли полностью клонировать вирусы SARS. Затем было показано, что эти клоны способны инфицировать клетки VeroE6 [20].
Когда были включены транскрипты N (нуклеокапсид), заражение было более сильным. Когда клетки не были инфицированы этим коронавирусом (контрольные клетки), окрашивание антителами к вирусу не наблюдалось.
Это же исследование показало, что ингибиторы цистеиновых протеиназ могут предотвратить заражение клеток. Оно также указало на то, что исследователи могут манипулировать генами вируса, по словам исследователей:
Текущие данные показывают, что ингибитор цистеиновой протеиназы E64-d может подавлять репликацию вируса SARS в любой момент во время заражения. … Доступность полноразмерной кДНК генома SARS должна позволить генетические манипуляции с геном репликазы, обеспечивая новое понимание роли специфических протеолитических расщеплений и белков репликазы во время репликации вируса [21].
Первая часть этого вывода в их исследовании ясно продемонстрировала интерес к дальнейшим генетическим манипуляциям с вирусом. Последняя часть имеет решающее значение для понимания возможности лечения SARS-CoV-2. Воздействие клиндамицина на эту трансмембранную протеазу серин 2 является одной из причин, по которым я решил включить его в лечение пациентов, инфицированных SARSCoV-2, и тех, кто испытывает воспалительно-тромбозную реакцию (ITR), известную как COVID-19 [22].
Структурный белок нуклеокапсида (N) вирусов SARS, по-видимому, не только играет значительную роль в повышении инфекционности, но также было показано, что для SARSCoV-2 он вставляет (обратно транскрибирует) свою генетическую последовательность в ДНК человека ― это также было профинансировано NIH, гранты 1U19AI131135-01, 5R01MH104610-21. С тех пор было показано, что эта обратная транскрипция (ОТ) встречается во всех, кроме трех, из двадцати трех пар хромосом человека [23].
2006: Химерная кДНК (усиление функциональности), полученная из вирусов гепатита С, ВИЧ-1, SARS-CoV-1 и SARS-CoV-2
В 2006 году китайские исследователи соединили четыре целевых сегмента кДНК вместе, чтобы сформировать единую последовательность РНК длиной 1200 нуклеотидов [24].
Эта химерная (усиление функциональности) последовательность включала комбинацию вируса гепатита С (HCV), вируса иммунодефицита человека - 1 (ВИЧ-1), SARS-CoV-1 и SARSCoV-2. Эта генетическая последовательность показана в приложении. Это исследование финансировалось правительством Фуцзяня [25] (номер гранта 2003Y004).
2007: Патент на геном SARS-CoV (SARS-CoV-1) [26] выдан министерству здравоохранения и социальных служб США
В мае 2007 года был выдан патент на выделение заражающего человека вируса SARS-CoV-1 [27]. Владельцем патента ― стороной, которая получит финансовую прибыль от патента, ― было Министерство здравоохранения и социальных служб США (HHS). Эта выделение не только генетически идентифицировала вирус, но также адаптировала тест полимеразной цепной реакции (ПЦР) для обнаружения SARSCoV-1. В апреле 2020 года FDA выдало всеобъемлющее разрешение на использование в чрезвычайных ситуациях (EUA) ПЦР-тестирования для выявления SARS-CoV-2 [28].
2007: Исследования показывают, что вставки, помещенные в белки-шипы, позволяют SARS-CoV инфицировать клетки людей
В исследовании, опубликованном доктором Чжэнли и исследователями из Австралийской лаборатории здоровья животных, были изучены SARS-подобные коронавирусы (SL-CoV), обнаруженные у подковоносых летучих мышей, и связанный с SARS коронавирус (SARS-CoV) [29]. Хотя они обнаружили значительное количество сходного генетического материала, они также обнаружили, что белок-шип SL-CoV не может связываться с человеческими рецепторами ACE2. Чжэнли и другие ученые обнаружили, что белок-шип у SL-CoV не может использовать рецепторы ACE2 для заражения человеческих клеток. Однако, когда они вставили аминокислоты, не встречающиеся в природных вирусах, в N-концевой домен посредством манипуляции с усилением функциональности (химерной), они обнаружили, что могут производить вирусы, способные инфицировать клетки человека.
2010: Ши Чжэнли-Ли проводит химерные эксперименты, показывающие, что белок-шип SARS-CoV не может связываться с рецепторами человеческих клеток ACE2
В 2010 году Ши Чжэнли провела химерное исследование на SARS-CoV-1 (тогда называемого SARS-CoV), включая объединение его с псевдовирусом ВИЧ для изучения связывающей способности этого вируса с человеческими рецепторами ACE2 [30]. Их работа, в частности, включала изменение (посредством мутагенеза) белков-шипов, чтобы определить, как увеличить связывание белков-шипов с рецептором ACE2.
Это исследование показало, что вставка пролин-аргинин-аргинин-аланин (PRRA) [31] не имеет решающего значения для связывания SARS-CoV-2 с рецепторами ACE2 на клетках человека. Как отмечается в этом опубликованном исследовании (совместно проведенном доктором Чжэнли из Уханьского института вирусологии, исследователями из Австралии и из Медицинской школы Университета Миннесоты), не только белок-шип [найденный в коронавирусах у] подковоносых летучих мышей не может связываться с рецепторами ACE2, но также эти различия наряду с различиями в циветах [32] подчеркивают критически важное недостающее звено в зоонозной теории происхождения SARS-CoV-2:
Однако, хотя генетически родственный SARS-подобный коронавирус (SL-CoV) был идентифицирован у подковоносых летучих мышей из рода Rhinolophus [5, 8, 12, 18], его белок-шип не мог использовать человеческий белок ACE2 (hACE2) в качестве рецептора. Тщательное изучение кристаллической структуры RBD SARS-CoV человека в комплексе с hACE2 предполагает, что укорочение области рецепторсвязывающего мотива (RBM) белка-шипа SL-CoV отменяет его hACE2-связывающую способность [7, 10], и, следовательно, SL-CoV, обнаруженный недавно у подковоносых летучих мышей, вряд ли является прямым предком SARS-CoV у человека.
Кроме того, было показано, что белок-шип человеческого SARS-CoV и наиболее близкий к нему белок-шип SARS-CoV у циветт не могли использовать ACE2 подковоносых летучих мышей (R. pearsoni) в качестве рецептора [13], что подчеркивает критически важное недостающее звено в цепи передачи SARSCoV от летучей мыши к циветте / человеку. [Выделение добавлено.]
2013: SARS-CoV был связан со смертельным свертыванием крови в легких
Барик и его сотрудники обнаружили в 2013 году, что SARSCoV ― в исследовании, финансируемом NIAID, NIH, Национальным центром развития междисциплинарных исследований (NIH / NCATS) и HHS (гранты HHSN272200800060C; 5UL1RR024140) ― имел четыре критических гена, которые были экспрессированы после инфицирования SARS-CoV:
Результаты этих исследований демонстрируют, что существует тонкий баланс между коагуляцией хозяина и путями фибринолизина, регулирующими патологические исходы заболевания, включая диффузное альвеолярное повреждение и острое повреждение легких, после заражения высокопатогенными респираторными вирусами, такими как SARS-CoV [33].
Далее они показали, что это имеет решающее значение для инфицирования и повреждения легких:
Каскад реакций урокиназы оказал значительное влияние как на патологию легких, так и на общий патогенез SARS-CoV.
Как показали исследования легочной ткани, чем больше вирусная нагрузка (более выраженная инфекция), тем больше повреждение легких фибрином (свертывание крови) [34].
2014: Барик подает заявку на международный патент на изменение белка-шипа коронавирусов
В марте 2014 года профессор Барик подал заявку на получение международного патента на методы получения и состав химерных (усиливающих функциональность) белков-шипов коронавируса. Как показано на следующем рисунке, это изобретение (патент) было создано при поддержке гранта NIH U54AI057157, что дополнительно демонстрирует, что федеральное правительство США финансирует исследование по усилению функциональности белка-шипа коронавируса.
Когда вы будете читать предыдущие абзацы, я рекомендую вам обратить особое внимание на слова, которые я выделил. Они дают интересное представление о том, что мы видели с 2019 года.
Предисловие здесь
Первая часть главы 1 здесь
Вторая часть главы 1 здесь
Перевод осуществлен членом РВС Иваном Ивановым.
Ссылки к главе 2
1. R. A. Flavell et al., “Site-Directed Mutagenesis: Generation of an Extracistronic Mutation in Bacteriophage QßRNA,” Journal of Molecular Biology 89, no. 2 (October 25, 1974): 255–72.
2. Charles Weissmann, “The End of the Road,” Landes Bioscience 6, no. 2 (2012): 970194, y.
3. M. M. Lai et al., “Recombination between Nonsegmented RNA Genomes of Murine Coronaviruses,” Journal of Virology 56 (1985): 449–56.
4. Kary B. Mullis et al., Process for Amplifying, Detecting, and/or Cloning Nucleic Acid Sequences, US Patent 4,683,195, 21; Tyler Durden, “Caught Red-Handed: CDC Changes Test Thresholds to Virtually Eliminate New COVID Cases among Vaxx’d,” ZeroHedge.com, May 23, 2021, https://www.zerohedge.com/covid-19/caught-red-handed-cdc-changes-test-th....
5. R. M. Fleming, “The Pathogenesis of Vascular Disease,” in Textbook of Angiology, ed. John C. Chang (New York: Springer Verlag, 1999), 787–98. doi:10.1007/978-1-4612-1190-7_64.
6. Хронические воспалительные заболевания включают болезнь коронарной артерии (болезнь сердца), сосудистую болезнь мозга (например, инсульт), гипертонию (высокое кровяное давление), сахарный диабет, ожирение и рак.
7. 20/20, April 16, 2004, “Hidden Heart Disease: Could a Simple, Inexpensive Test Save Your Life?,” aired April 16, 2004, on ABC; https://rumble.com/vkb7n1-inflammation-and-heart-disease-2020.html.
8. Richard M. Fleming and Matthew R. Fleming, “FMTVDM Quantitative Nuclear Imaging Finds Three Treatments for SARSCoV-2,” Biomedical Journal of Scientific and Medical Research 33, no. 4 (February 8, 2021): 26041– 83, doi:10.26717/BJSTR.2021.33.005443, https://biomedres.us/fulltexts/BJSTR.MS.ID.005443.php.
9. F. Almazán, “Engineering the Largest RNA Virus Genome as an Infectious Bacterial Artificial Chromosome,” Proceedings of the National Academy of Sciences 97, no. 10 (2000): 5516–21.
10. Ibid.
11. Boyd Yount, Kristopher M. Curtis, and Ralph S. Baric, “Strategy for Systematic Assembly of Large RNA and DNA Genomes: Transmissible Gastroenteritis Virus Model,” Journal of Virology 74, no. 22 (December 22, 2000): 10600–11.
12. Ibid.
13. Volker Thiel et al., “Infectious RNA Transcribed In Vitro from a cDNA Copy of the Human Coronavirus Genome Cloned in Vaccinia Virus,” Journal of General Virology 82 (June 2001): 1273–81.
14. Клетки MRC-5 (также известные как линия клеток № 5 Совета по медицинским исследованиям) была выращена из легочной ткани 14-недельного аботированного мужского зародыша европеоида.
15. Один из способов сделать это - это кластеры коротких палиндромных повторов с регулярными интервалами. One method for doing this is called Clusters of Regularly Interspaced Short Palindromic Repeats (CRISPR).
16. Bredenbeek and Rice, 1992; Mandl et al., 1998.
17. Boyd Yount, Kristopher M. Curtis, and Ralph S. Baric, “Strategy for Systematic Assembly of Large RNA and DNA Genomes: Transmissible Gastroenteritis Virus Model,” Journal of Virology 74, no. 22 (December 22, 2000): 10600–11.
18. Boyd Yount et al., “Reverse Genetics with a Full-Length Infectious cDNA of Severe Acute Respiratory Syndrome Coronavirus,” Proceedings of the National Academy of Sciences 100, no. 22 (October 28, 2003): 12995–13000.
19. Возможность использовать обратную транскрипцию для получения кДНК из мРНК. The ability to use reverse transcription to make cDNA from mRNA.
20. Клетки Vero E6 ― линия клеток эпителия почек, взятых у африканской зеленой мартышки 27 марта 1962 года.
21. Boyd Yount et al., “Reverse Genetics with a Full-Length Infectious cDNA of Severe Acute Respiratory Syndrome Coronavirus,” Proceedings of the National Academy of Sciences 100, no. 22 (October 28, 2003): 12995–13000.
22. NCT04349410. Richard M. Fleming and Matthew R. Fleming, “FMTVDM Quantitative Nuclear Imaging Finds Three Treatments for SARS-Cov-2,” Biomedical Journal of Scientific and Medical Research 33, no. 4 (February 8, 2021): 26041–83, doi: 10.26717/BJSTR.2021.33.005443, https://biomedres.us/fulltexts/BJSTR.MS.ID.005443.php; Canrong Wu et al., “Analysis of Therapeutic Targets for SARS-CoV-2 and Discovery of Potential Drugs by Computational Methods,” Acta Pharmaceutica Sinica B 10, no. 5 (May 2020): 766–88; Satish Sagar et al., “Bromelain Inhibits SARS-CoV-2 Infection via Targeting ACE-2, TMPRSS2, and Spike Protein,” Clinical and Translational Medicine 11, no. 2 (February 2021): e281.
23. Liguo Zhang et al., “Reverse Transcribed SARS-CoV-2 RNA Can Integrate into the Genome of Cultured Human Cells and Can Be Expressed in Patient-Derived Tissues,” Proceedings of the National Academy of Sciences 118, no. 21 (May 25, 2021): e2105968118.
24. Qiuying Huang et al., “Preparation of Chimeric Armored RNA as a Versatile Calibrator for Multiple Virus Assays,” Clinical Chemistry 52, no. 7 (July 1, 2006): 1446–48 and Supplement A.
25. Commonly known as the People’s Revolutionary Government of the Republic of China. Since 2018, it has been superseded and duties transferred to the Kinmen-Matsu Joint Services, the National Development Council, and other ministries for the Executive Yuan (executive branch) of Taiwan.
26. Genome is the entire genetic code of an organism—for example, the SARSCoV-1 virus.
27. US Department of Health and Human Services, Coronavirus Isolated from Humans, Patent 7,220,852 B1, issued May 22, 2007.
28. US Food and Drug Administration, “In Vitro Diagnostics EUAs — Molecular Diagnostic Tests for SARS-CoV-2,” last updated July 19, 2021, https://www.fda.gov/medical-devices/coronavirus-disease-2019-covid-19-em....
29. Wuze Ren et al., “Difference in Receptor Usage between Severe Acute Respiratory Syndrome (SARS) Coronavirus and SARS Like Coronavirus of Bat Origin,” Journal of Virology 82, no. 4 (February 2008): 1899–1907.
30. Yuxuan Hou et al., “Angiotensin-Converting Enzyme 2 (ACE2) Proteins of Different Bat Species Confer Variable Susceptibility to SARS-CoV Entry,” Archives of Virology 155, no. 10 (October 2010): 1563–69, doi: 10.1007/ s00705-010-0729-6.
31. PRRA ― буквенное обозначение четырех аминокислот, в частности пролина, аргинина, аргинина и аланина.
32. Asian-African animal species frequently used by those like Daszak who attempt to explain SARS-CoV-2 as a naturally occurring (zoonotic) virus.
33. Lisa E. Gralinski et al., “Mechanisms of Severe Acute Respiratory Syndrome Coronavirus-Induced Acute Lung Injury,” mBio 4, no. 4 (August 6, 2013): e00271-13, doi:10.1128/mBio.00271-13.
34. Ibid.
35. TMPRSS2 is transmembrane protease serine 2. This enzyme, which breaks apart proteins, is found in humans. The gene for TMPRSS2 is found on human chromosome 21. See https://doi.org/10.1006/geno.1997.4845.
36. Xue Han et al., “Structure of the S1 Subunit C-Terminal Domain from Bat-Derived Coronavirus HKU5 Spike Protein,” Virology 507 (July 2017): 101–9.
37. Y. Yang et al., “Receptor Usage and Cell Entry of Bat Coronavirus HKU4 Provide Insight into Bat-to-Human Transmission of MERS Coronavirus,” Proceedings of the National Academy of Sciences 111, no. 34 (August 26, 2014): 12516–21.
38. R. M. Fleming, “The Pathogenesis of Vascular Disease,” in Textbook of Angiology, ed. John C. Chang (New York: Springer Verlag, 1999), 787–98. https://doi.org/10.1007/978-1-4612-1190-7_64.
39. William T. Gibson et al., “ACE 2 Coding Variants: A Potential XLinked Risk Factor for COVID-19 Disease,” BioRXiv (April 14, 2020), https://doi.org/10.1101/2020.04.05.026633.
40. Wanbo Tai et al., “Characterization of the Receptor-Binding Domain (RBD) of 2019 Novel Coronavirus: Implications for Development of RBD Protein as a Viral Attachment Inhibitor and Vaccine,” Cellular & Molecular Immunology 17, no. 6 (June 2020): 613–20.
41. SARS-CoV, now referred to as SARS-CoV-1, was first reported in China in February of 2003. See https://www.cdc.gov/sars/index.html.
42. “Lethal Deception,” Rumble.com, April 22, 2021. Video, 1:31:19, https://rumble.com/vfy3xf-lethal-deception.html.
43. Boyd Yount et al., “Reverse Genetics with a Full-Length Infectious cDNA of Severe Acute Respiratory Syndrome Coronavirus,” Proceedings of the National Academy of Sciences 100, no. 22 (October 28, 2003): 12995–13000; M. M. Becker, “Synthetic Recombinant Bat SARS-Like Coronavirus Is Infectious in Cultured Cells and in Mice,” Proceedings of the National Academy of Sciences 105, no. 50 (December 2008): 19944–49.
44. V. D. Menachery et al., “A SARS-Like Cluster of Circulating Bat Coronaviruses Shows Potential for Human Emergence,” Nature Medicine 21, no. 12 (2015): 1508–13.
45. “New SARS-Like Virus Can Jump Directly from Bats to Humans, No Treatment Available,” Gillings School of Global Public Health, November 9, 2015, https://sph.unc.edu/sph-news/new-sars-like-virus-can-jump-directly-from-....
46. That’s something Dr. Fauci now denies (see https://twitchy.com/samj-3930/2021/05/11/its-on-dr-fauci-did-not-like-se...), despite the publication acknowledging NIAID funding.
47. V. D. Menachery et al., “Corrigendum: A SARS-Like Cluster of Circulating Bat Coronaviruses Shows Potential for Human Emergence,” Nature Medicine 22, no. 4 (2016): 446.
48. Gordon Duff, “Documentary Proof: University of North Carolina Generated COVID-19,” State of the Nation (website), April 28, 2020, https://stateofthenation.co/?p=12668.
49. V. D. Menachery et al., “A SARS-Like Cluster of Circulating Bat Coronaviruses Shows Potential for Human Emergence,” Nature Medicine 21, no. 12 (2015): 1508–13, doi:10.1038/nm.3985.
50. Dr. Carlo Urbani was an Italian microbiologist and physician who first identified Severe Acute Respiratory (SARS) viruses and warned the WHO.
51. A = adenine, C = cytosine, G = guanine, T = thymine, and U (not shown here) = uracil.
52. Richard M. Fleming, Unmasking COVID — Part 1 (self-pub., 2020), Kindle, https://www.amazon.com/Unmasking-CoViD-Dr-Richard-Fleming-ebook/dp/B08N5....
53. V. D. Menachery et al., “A SARS-Like Cluster of Circulating Bat Coronaviruses Shows Potential for Human Emergence,” Nature Medicine 21, no. 12 (2015): 1508–13.
54. V. D. Menachery et al., “Corrigendum: A SARS-Like Cluster of Circulating Bat Coronaviruses Shows Potential for Human Emergence,” Nature Medicine 22, no. 4 (2016): 446.
55. Bill Gates said it would be a “‘tragedy’ to pass up a controversial, revolutionary gene-editing technology.” Article by Kevin Loria April 12, 2018 Insider.
56. Janet Levy, “Mengele’s Unethical Research Was Part of Existing Beliefs, Practice,” Jerusalem Post, August 6, 2020, https://www.jpost.com/israel-news/culture/mengeles-unethical-research-wa....
57. Y. Yang et al., “Two Mutations Were Critical for Bat-to-Human Transmission of Middle East Respiratory Syndrome Coronavirus,” Journal of Virology 89, no. 17 (2015): 9119–23.
58. Ibid.
59. C. Calisher et al,, “Statement in Support of the Scientists, Public Health Professionals, and Medical Professionals of China Combating Covid-19,” Lancet 395 (2020): e42-43.
60. Zoonotic viruses are viruses spread from animals to people. See https://www.cdc.gov/onehealth/basics/zoonotic-diseases.html.
61. Andrew Kerr, “US Researcher with Chinese Ties Admits He Convinced WHO Team That Missing Wuhan Lab Data Was Irrelevant,” Daily Caller, March 10, 2021, https://dailycaller.com/2021/03/10/who-investigators-wuhan-lab-database-....
62. Sam Husseini, “EcoHealth Alliance Has Hidden Almost $40 Million in Pentagon Funding and Militarized Pandemic Science,” Independent Science News (website), December 16, 2020, https://www.independentsciencenews.org/news/peter-daszaks-ecohealth-alli....
